Struktura przewodu pokarmowego.
Funkcją przewodu pokarmowego jest przyjmowanie, trawienie, wchłanianie i wydalanie niestrawionych resztek jedzenia. Ale czy wiesz, że ponad 70% twojego układu odpornościowego jest tam zlokalizowane? Jedząc codziennie, dostarczamy naszemu organizmowi bakterie, wirusy, drożdże i pasożyty. Możliwe także toksyny, metale ciężkie lub inne chemikalia. Stały kontakt mikrobiomu jelitowego z układem GALT jest niezbędny do utrzymania odpowiedniej odpowiedzi immunologicznej. Jelito jest tak autonomiczne, że ma własny układ odpornościowy i nerwowy. Układ odpornościowy jelit to tkanka limfatyczna połączona z błoną śluzową jelit, tzw. GALT (gut associated lymphoid tissue -tkanka limfatyczna związana z jelitami). GALT jest częścią centralnego układu limfatycznego połączonego z błonami śluzowymi, tzw. MALT (mucosa associated lymphoid tissue – tkanka limfatyczna związana z błoną śluzową) i zapewnia silną miejscową ochronę błony śluzowej. Składniki morfologiczne MALT to skupiska tkanki limfatycznej (guzki limfatyczne) oraz warstwy błony śluzowej i podśluzowej.
Tkanka limfatyczna związana z GALT zawiera ponad 70% limfocytów całego układu odpornościowego, w których limfocyty B wydzielające śluzowe przeciwciała IgA są najliczniejszą grupą.
Kliknij na zdjęcie, aby powiększyć. Zastrzegam prawa autorskie do obrazu. Kopiowanie i rozpowszechnianie bez mojej zgody jest zabronione.
GALT składa się z:
Komponenty fizyczne.
- mikrobiom jelitowy – znany również jako bakterie komensalne. Chronią przed szkodliwym lub patogennym wzrostem bakterii. Współzawodniczą ze złymi bakteriami o substancje odżywcze i uwalniają substancje przeciwdrobnoustrojowe. Dobre bakterie regulują również proces trawienia i wchłaniania substancji krytycznych dla organizmu. Są w stanie wytwarzać krótkie kwasy tłuszczowe, które dostarczają energii do ochronnych komórek nabłonkowych jelita. Mogą również stymulować komórki kubkowe (GC) do zwiększania grubości powierzchni mucyny. Im mniejsza ilość dobrych bakterii, tym cieńsza warstwa błony śluzowej i mniejsza ochrona przed inwazją patogenów na układ odpornościowy gospodarza. Może to prowadzić do stanów zapalnych i chorób zapalnych. Bakterie komensalne lub ich produkty, takie jak lipopolisacharyd (LPS) i peptydoglikan, mają zdolność przywracania warstwy śluzu. Liczebność mikrobiomu odgrywa dużą rolę w odnowie komórek nabłonka jelitowego. W przypadku „nieszczelnego jelita” bakterie w świetle jelita i ich produkty mogą dotrzeć do blaszki właściwej i wywołać stan zapalny. Przeniesienie do krążenia obwodowego może spowodować uszkodzenie tkanek i autoimmunizację.
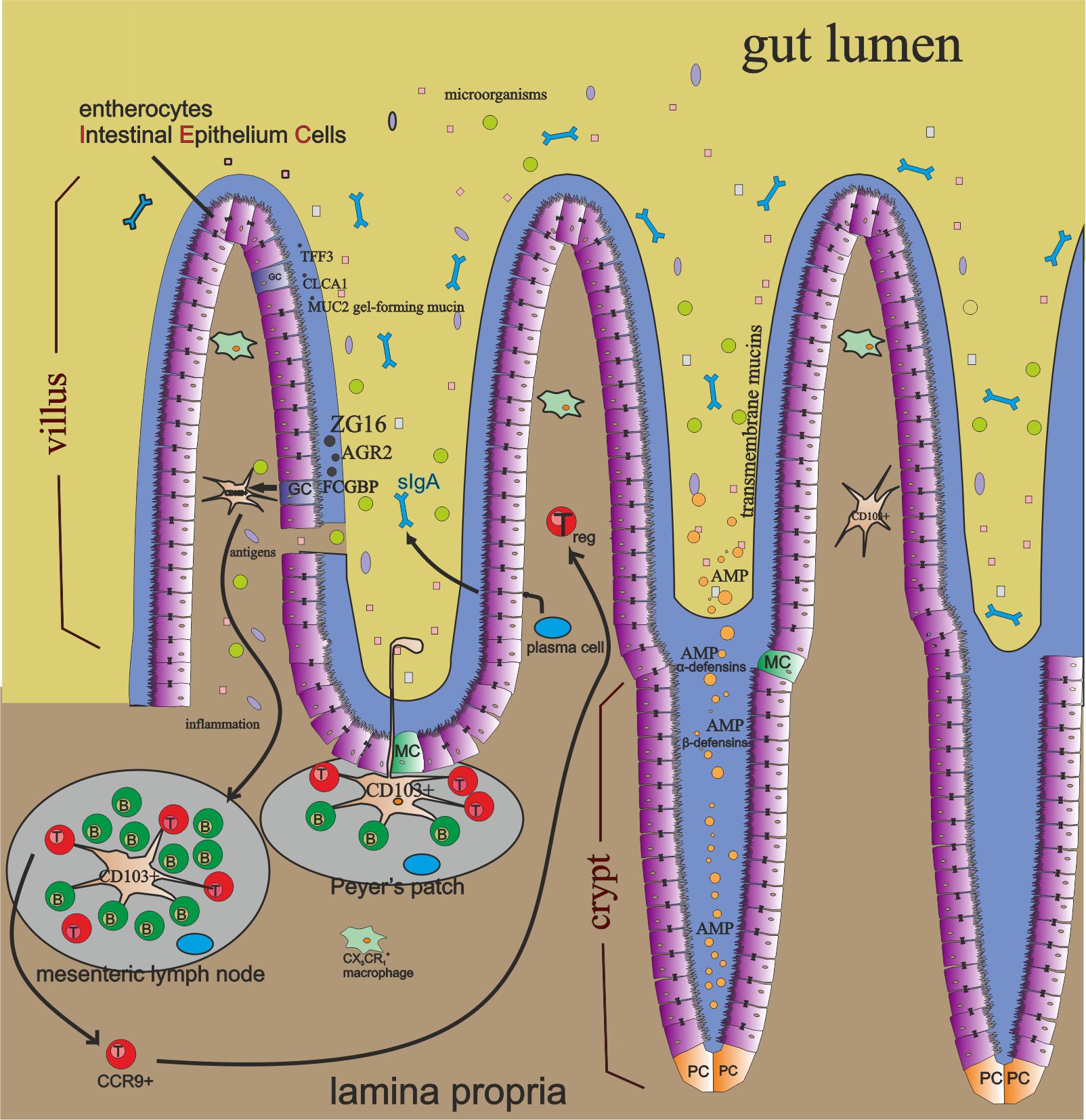
- wewnętrzna i zewnętrzna warstwa śluzu pokrywająca komórki nabłonkowe jelita. Jego głównym składnikiem jest mucyna żelotwórcza (MUC2) wytwarzana przez komórki kubkowe (GC). Śluz zawiera wiele cząsteczek, takich jak IgA, enzymy i białka.
- Komórki nabłonkowe jelita (IEC), które mogłyby pokryć nawet 400 m² powierzchni. Komórki są odnawiane co 3-5 dni, nie licząc komórek Paneth-a,o żywotności około dwóch miesięcy. Wszystkie komórki nabłonkowe są wytwarzane z jelitowych komórek macierzystych, które są ukryte na samym dnie krypt Lieberkün-a.
-
- Enterocyty – najliczniejszy typ IEC, około 90% wszystkich komórek. Odpowiadają za pobieranie składników odżywczych i kontrolę populacji bakterii Gram-dodatnich poprzez ekspresję białek przeciwdrobnoustrojowych (RegIIIγ). Wytwarzają również mucyny międzybłonowe.
- Komórki kubkowe (GC) – wytwarzają mucynę MUC2 i inne składniki śluzu. Prezentują także antygeny komórkom dendrytycznym CD103 + w blaszce właściwej w jelicie cienkim, tworząc luki (GAP – goblet cell-associated passages). Te komórki i GAP, które one tworzą mogą wykrywać i hamować translokację inwazyjnych patogenów do układu odpornościowego gospodarza.
- Komórki Paneth-a – (PC) – wytwarzają białka przeciwdrobnoustrojowe (AMP – antimicrobial proteins): α-defensyny, β-defensyny, lektyny typu C, katelicydyna, lizozym, jelitowa fosfataza alkaliczna (IAP – intestinal alkaline phosphatase) – mogą inaktywować LPS, zapobiegać translokacji przez nabłonek i regulować białka połączeń ścisłych (Tj – tight junctions) żeby zwiększyć białko Zonula occludens ZO-1 (Tj-1) i ZO-2 (Tj-2), Ang4 – bakterie Bacteroides thetaiotaomicron pobudzają komórki paneth-a do wytwarzania tego białka przeciwmikrobowego (AMP). Drobnoustroje oddziałują z tymi substancjami.
- Komórki M -komórki z mikro-pofałdowaniami ( MC – microfold cells)) – transportują antygeny (w procesie nazywanym transcytozą) przez cytoplazmę komórek nabłonka jelitowego do zlokalizowanych poniżej kępek Peyera.
- komórki enteroendokrynne
- komórki kubkowe
- komórki pędzęlkowate
-
- Połączenia ścisłe (Tj – tight junctions) – komórki nabłonkowe jelit tworzą ciągłe połączenie i są uszczelnione przez ścisłe połączenia białek. Taki transfer substancji przez jelita przez przestrzenie między komórkami nabłonka nazywa się przepuszczalnością międzykomórkową i może być zwiększony przez warunki patologiczne. Zonula occludens jest jednym z takich białek.
Komponenty biochemiczne.
Składniki te mają właściwości przeciwdrobnoustrojowe i występują w śluzie, świetle jelita i zawierają kwasy żółciowe. Ich rolą jest ochrona przed kontaktem drobnoustrojów, toksyn i innych antygenów światła z komórkami gospodarza. Im większa odległość od żołądka, tym pH rośnie. Oczywiście, im bardziej skolonizowany mikrobiom w przewodzie pokarmowym i tym więcej białek przeciwdrobnoustrojowych (AMP) jest wytwarzanych.
Komponenty immunologiczne.
- kępki Peyer-a – grupy pęcherzyków limfatycznych w błonie śluzowej wyściełającej jelito cienkie (zagregowane guzki limfoidalne). Kontrolują populacje bakterii jelitowych i zapobiegają rozwojowi bakterii chorobotwórczych.
- makrofagi – rodzaj białych krwinek, które jako pierwsze docierają do miejsca infekcji. Rozróżniamy dwa typy: M1 i M2. M1 stymuluje układ odpornościowy do walki poprzez zwiększenie stanu zapalnego. W procesie zwanym fagocytozą pochłaniają i trawią zainfekowane komórki. Ale najpierw muszą przejść procesy biochemiczne, aby się aktywować. Aktywowany makrofag jest bardziej cytotoksyczny i ma inną strukturę komórkową. Komórki M2 mają zdolność uwalniania cytokin przeciwzapalnych, które zmniejszają zapalenie w ciele. Jednojądrzaste fagocyty jelitowe, takie jak makrofagi CX3CR1 +, są w stanie wykryć zawartość światła jelita. Ponadto te komórki eksprymujące mogą próbkować antygeny przez tworzenie struktur przeznabłonkowych (TED) w zależności od chemokiny CX3CL1, wydzielanej przez niektóre komórki nabłonka jelitowego.
- komórki plazmatyczne – przebywają w blaszce jelitowej i wytwarzają sIgA w ilości 50 mg / kg ciała dziennie!
- wydzielnicze IgA (sIgA – secretory immunoglobulin A) – immunoglobulina, która znajduje się głównie na powierzchniach błony śluzowej jelit i jest bardzo ważna dla ochrony organizmu przed patogenami. W porównaniu z innymi izotypami przeciwciał, jej szczególną cechą jest to, że w środowisku bogatym w proteazy nie traci swojej funkcji i pozostaje aktywna. Immunoglobuliny IgA mogą być transcytozowane przez nabłonek i wydzielane w świetle jelita. IgA wydzielnicza wiąże się z bakteriami i wirusami, które dostały się do przewodu pokarmowego i oskrzeli, i pomaga usunąć je z organizmu. Jako substancja wydzielana do światła jelita w określonym stężeniu może być wskaźnikiem jelitowym (markerem) stanu jelit.
- komórki dendrytyczne.
Cieknące jelito i związek z reakcją autoimmunologiczną.
Translokacja.
Wiele chorób wiąże się ze zmienionym i słabym mikrobiomem jelitowym (choroba Alzheimera, alkoholowa choroba wątroby, rak i wiele chorób autoimmunologicznych),z dysbiozą, z zaburzeniami bariery jelitowej i translokacją drobnoustrojów. Translokacja prowadzi do wytworzenia autoprzeciwciał przeciwko własnym antygenom, które niszczą własne tkanki organizmu. Komórki M transportują (transportują przez cytoplazmę) antygeny ze światła jelita przez nabłonek jelitowy do kępek Peyer-a w blaszce właściwej w jelicie cienkim. Obserwuje się także prezentację antygenów jelitowych komórkom dendrytycznym CD103 + przez komórki kubkowe w blaszce właściwej. Powstają połączenia antygenów związane z komórkami kubkowymi (GAP) (kanały jonowo-metaboliczne???). Komórki kubkowe i GAP są w stanie rozpoznać patogennych najeźdźców i zahamować ich penetrację w kierunku układu odpornościowego gospodarza.
Bakterie komensalne.
Bakterie komensalne i warstwa śluzu przyczyniają się do utrzymania zjawiska homeostazy. Warstwa śluzu jest bogata w białka przeciwdrobnoustrojowe (AMP, na przykład RegIIIγ wytwarzane przez enterocyty), które pozwalają układowi immunologicznemu kontrolować mikrobiotę, a mikrobiota uwalnia niektóre produkty metaboliczne, które hamują układ odpornościowy gospodarza. Relokacja bakterii i ich produktów może powodować nieprawidłową odpowiedź immunologiczną. Zwiększona przepuszczalność nabłonka indukuje stan zapalny. Czynnikami, które uruchamiają ten mechanizm nieszczelności jelit i translokację mikrobów ze światła jelita, mogą być: dieta, infekcje, spożywanie alkoholu, oparzenia,stres itp.
Jak zmniejszyć przepuszczalność jelit i naprawić nieszczelne jelita?
Utrzymując zdrowe jelita, wzmacniając połączenia białek połączeń ścisłych (Tj), wspomagając odnowę komórek nabłonka jelitowego i zwiększając liczbę bakterii komensalnych, aby utrzymać grubą warstwę błony śluzowej! Cofanie objawów nieszczelnego jelita może byćobiecującą strategią terapeutyczną!
1. Zoptymalizuj swoją dietę ponieważ to 70% Twojego sukcesu! Ja czuję się najlepiej kiedy spożywam bezglutenowe, ubogie w dodane oleje i wegańskie pokarmy – ale zdrowe jedzenie. Posiłki przygotowane w domu, bogate w świeże warzywa i owoce, żaden fast food oznakowany jako wegański. Kliknij w wybrany link, żeby znaleźć coś naprawdę odżywczego i zdrowego! W przypadku, kiedy chcesz popełnić mały grzech, kliknij tutaj!
2.Bardzo ważna Witamina D została zidentyfikowana jako protektor przepuszczalnoiści jelitowej.Ta witamina indukuje ekspresję białek połączeń ścisłych (Tj) takich jak ZO-1 i klaudyna-1.
3. Naukowcy dowiedli, że dieta uboga w błonnik może wyzwalać przerost populacji bakterii niszcząc grubość warstwy śluzowej (Akkermansia muciniphila, Bacteroides caccae)
4. Dieta bogata w tłuszcze wysokonasycone prowadzi do zmniejszenia ilości bakterii z grupyLactobacillus, zwiększa Oscilibacter (olej kokosowy z pierwszego tłoczenia jest kontrowersyjny)
5. Obfitość Oscilospirra osłabia błonę śluzową zwiększając przepuszczalność poprzez formowanie ZO-1.
6. Stres może powodować zwiększoną przepuszczalność jelitową, toteż zmiany mikrobiomu i jego liczebności populacji tlenowych i beztlenowych bakterii produkujących maślan zmniejsza się w kale.
7. Alkohol zmienia jakość i ilość mikrobiomu, indukuje translokację lipopolisacharydu (LPS)oraz alkoholową chorobę wątroby. Tłumi Lactobacillus a także zaburza integralność błony śluzowej. Niektóre bakterie takie jak e.coli mogą same produkować alkohol, dlatego jest to powód dla którego mogą żyć w jelicie. Picie alkoholu może tłumić aktywność RegIIIγ , jednak suplementacja Lactobacilli and Bifidobacteria może przywrócić funkcje RegIIIγ. E. coli są LPS-produktywnymi bakteriami a Bifidobacterium kontroluje je.
8. Przeszczep mikrobiomu może pomóc przebudować przesiąkliwe jelito i wzmocnić barierę ochronną.
9. Probiotyki które nie rozpuszczają się w żołądku oraz prebiotyki – pokarmy, które karmią dobre bakterie w jelicie mogą zredukować przepuszczalność jelitową. Zastosowanie Bacteroides fragilis do zapobiegania zjawisku przesiąkliwego jelita i cofania chorób autoimmunologicznych jest obiecujące, wymaga jednak dalszego badania.
10. Żywe probiotyki na świezych warzywach i owocach (to jest aspekt teorii spożywania brudnego jedzenia)
11. Kiełki – pomagają skolonizować jelito kręte unikalnymi gatunkami bakterii
Podoba Ci się post?
Polub i obserwuj moją stronę na facebook-u (https://www.facebook.com/vitaminove/). Najpierw należy kliknąć Lubię to! a następnie w opcjach obserwowania ustawić „wyświetlaj najpierw”
Zajrzyj również na mój Instagram (https://www.instagram.com/vitaminove_com/)
Zostaw komentarz!
Proszę udostępnij przyciskiem poniżej!
Bibliography:
- dr n. med. Mirosława Gałęcka, “Dieta w chorobach autoimmunologicznych”, PZWL Wydawnictwo lekarskie.
- Dr n. med. B. Sieradzka, „Znaczenie układu odpornościowego przewodu pokarmowego dla organizmu„.
- Qinghui Mu, imageJay Kirby, imageChristopher M. Reilly and imageXin M. Luo,; Leaky Gut As a Danger Signal for Autoimmune Diseases.
- Arndt Manzel, Dominik N. Muller, David A. Haffler, Susan E. Erdman, Ralf A. Linker, M, Markus Kleinewietfeld, Role of Western Diet in inflammatory autoimmune diseases.
- Helena Tlaskalová-Hogenová, Renata Štěpánková, Hana Kozáková, Tomáš Hudcovic, Luca Vannucci, Ludmila Tučková, Pavel Rossmann, Tomáš Hrnčíř, Miloslav Kverka, Zuzana Zákostelská, Klára Klimešová, Jaroslava Přibylová, Jiřina Bártová, Daniel Sanchez, Petra Fundová, Dana Borovská, Dagmar Šrůtková, Zdeněk Zídek, Martin Schwarzer, Pavel Drastich & David P Funda, The role of gut microbiota (commensal bacteria) and the mucosal barrier in the pathogenesis of inflammatory and autoimmune diseases and cancer: contribution of germ-free and gnotobiotic animal models of human diseases.
- Yan Y. Lam*, Connie W. Y. Ha, Craig R. Campbell, Andrew J. Mitchell, Anuwat Dinudom, Jan Oscarsson, David I. Cook, Nicholas H. Hunt, Ian D. Caterson, Andrew J. Holmes, Len H. Storlien, Increased Gut Permeability and Microbiota Change Associate with Mesenteric Fat Inflammation and Metabolic Dysfunction in Diet-Induced Obese Mice.








Komentarze
Pingback: Samoleczenie choroby autoimmunologicznej dietą i stylem życia. - vitaminove.com